Produire de nouveaux
savoirs
Explorer de nouvelles avenues pour développer la connaissance médicale de demain dans une approche qui intègre recherche fondamentale et recherche clinique.
Nos groupes de recherche sont dirigés par des chercheuses et chercheurs principaux qui collaborent dans un esprit de collégialité et de partage pour rapprocher la recherche des patients et patientes et former la relève scientifique. Ce sont des esprits libres et indépendants qui travaillent sans relâche pour améliorer la santé. Découvrez les chercheurs et chercheuses de l'IRCM.
Recherche en cours
"Notre travail vise à déterminer comment l'échange local de signaux entre cellules contribue à la croissance et à l'organisation normales des tissus épithéliaux."
David Hipfner, directeur de recherche
Biologie des cellules épithéliales
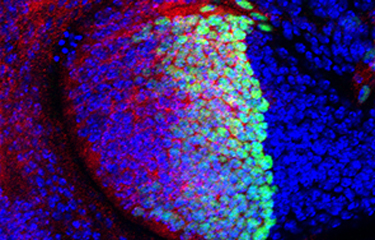
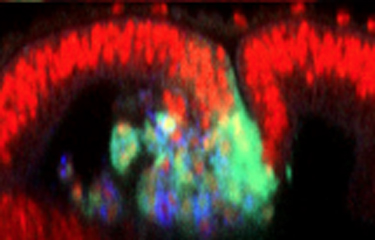
Les cellules épithéliales sont l’une des composantes fondamentales des tissus animaux. Ces cellules hautement spécialisées sont étroitement liées les unes aux autres pour former des feuillets épithéliaux ou épithéliums. Les épithéliums délimitent les surfaces interne et externe des organes, ainsi que les interfaces entre les tissus. Les cellules épithéliales servent à diverses fonctions essentielles telles que la protection (la peau), la sécrétion (différentes glandes) et l’absorption (des intestins). De plus, elles procurent des surfaces pour l’échange des gaz (dans les poumons et les vaisseaux sanguins). L’étendue de leurs fonctions suscite beaucoup d’intérêt chez les chercheurs qui aimeraient comprendre comment se forment les tissus épithéliaux et comment ils maintiennent leur structure.
Le but visé de l'unité de recherche en biologie des cellules épithéliales est l’apport de connaissances sur les mécanismes de base indispensables à la formation, à la croissance et au modelage des tissus épithéliaux pendant le développement embryonnaire. Vu le rôle primordial que joue la dérégulation de la prolifération, de la survie et de l’organisation cellulaires dans le cancer, l’unité de recherche espère ainsi acquérir une meilleure compréhension des mécanismes impliqués dans la formation des tumeurs et des métastases chez l’humain.
| Équipe |
|
| Affiliations |
|
| Formations et expérience |
|
Mécanismes contrôlant le façonnage et la croissance des tissus épithéliaux
La drosophile - un excellent système modèle pour étudier la croissance et le façonnage des tissus
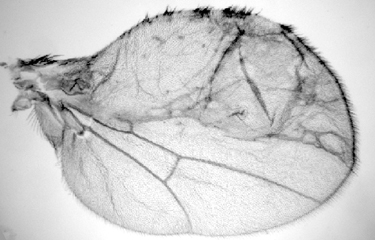
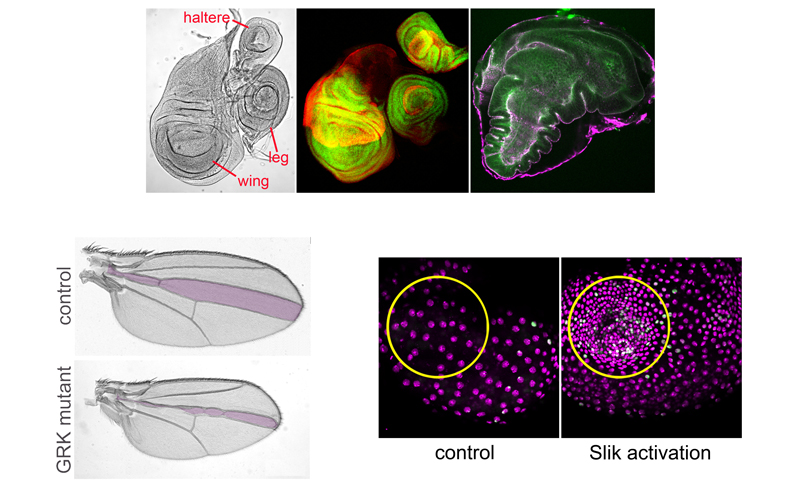
La mouche à fruit Drosophila melanogaster offre un certain nombre davantages qui en ont fait l'un des organismes modèles les plus populaires pour les études génétiques du développement et des maladies. Malgré nos différences, de nombreux processus et gènes importants pour le développement humain sont conservés chez la drosophile. Nous nous concentrons sur le développement des disques imaginaux, qui sont de petits sacs épithéliaux formés dans l'embryon qui se développent rapidement pour former des structures comme les yeux, les ailes et les pattes. En raison de leur structure simple, de leur croissance rapide et de leur accessibilité facile, les disques imaginaux sont un système idéal pour étudier comment la croissance et le façonnage des tissus épithéliaux sont contrôlées.
Façonnage
La voie de signalisation Hedgehog joue un rôle central dans l'organisation de la plupart des tissus embryonnaires et est mal régulée dans de nombreux cancers. Nous avons découvert que les kinases couplés aux récepteurs protéines G (GRK) jouent un rôle important dans le contrôle de l'activité de cette voie, les mouches mutantes GRK présentant un façonnage alaire anormal. Nous avons lié cela à une dérégulation plus large des récepteurs couplés aux protéines G et nous travaillons à déterminer les manières complexes dont cela affecte la sortie de la voie Hedgehog.
Croissance
Nous avons montré qu'une protéine kinase appelée Slik est capable d'accélérer la croissance des tissus chez la drosophile, de la même manière que certains oncogènes humains favorisant la croissance des tumeurs. Slik assure la médiation d'un échange local de signaux entre les cellules qui provoque la croissance et la division des cellules réceptrices. Nous avons identifié plusieurs facteurs qui contrôlent cette activité de Slik, et nous travaillons à comprendre comment ils le font et par quel mécanisme les cellules exprimant Slik stimulent la croissance des cellules voisines.
Découvertes importantes
|
2021 Extensive crosstalk of G protein-coupled receptors with the Hedgehog signalling pathway |
|
2020 STRIPAK regulates Slik localization to control mitotic morphogenesis and epithelial integrity |
|
2015 Regulation of Catalytic and Non-catalytic Functions of the Drosophila Ste20 Kinase Slik by Activation Segment Phosphorylation |
|
2014 A broadly conserved G protein-coupled receptor kinase phosphorylation mechanism controls Drosophila smoothened activity |
Outils
| Revue de presse |
| Revue de presse |
| Subventions |
| Reconnaissances et honneur |
Rejoindre
le groupe
de recherche
Postes disponibles
Études cliniques en cours
Partenaires de recherche


Contacter le
groupe de recherche
514 987-5508
david.hipfner@ircm.qc.ca
La vie au
laboratoire

© Institut de recherches cliniques de Montréal, Année.Tous droits réservés. | Politique sur la protection des renseignements personnels | Conditions d'utilisation | Réalisation Agence Riposte